太陽は銀河系の中では主系列星の一つで、スペクトル型はG2V(金色)である。
| 痛風 | |
|---|---|
| 他の名前 | 足の関節炎(尿路性関節炎、または足部痛) |
| ビデオ要約(スクリプト)。主役は『痛風』(ジェームズ・ギルレイ、1799年)で、この作品では、痛風による痛みが悪魔や竜として描かれている。[1] [2] | |
| 専門 | リウマチ学 |
| 症状 | 関節の痛み、腫れ、赤み[3] |
| 通常の発症 | 高齢男性[3] 、閉経後女性[4] |
| 原因 | 尿酸[4] |
| 危険因子 | 肉やビールを多く摂取する食事、太りすぎ、遺伝[3] [5] |
| 鑑別診断 | 関節感染症、関節リウマチ、偽痛風、その他[6] |
| 防止 | 減量、禁酒、アロプリノール[7] |
| 処理 | NSAIDs、グルココルチコイド、コルヒチン[4] [8] |
| 頻度 | 1~2%(先進国)[7] |
痛風(/ ɡ aʊ t / GOWT [9] )は、炎症性関節炎の一種で、関節が赤くなり、圧痛があり、熱を持ち、腫れ、痛みが繰り返し起こるのが特徴です。[4] [10]原因は、尿酸ナトリウム結晶と呼ばれる針状の尿酸結晶の沈着です。[11]痛みは通常急速に現れ、12時間以内に最大強度に達します。[7]約半数の症例で、親指の付け根の関節が影響を受けます(足部痛)。[12] [13]また、痛風結節、腎臓結石、または腎臓障害を引き起こすこともあります。[3]
痛風は、血液中の尿酸(尿酸塩)のレベルが持続的に上昇することで起こります(高尿酸血症)。[4] [7]これは、食事、他の健康問題、遺伝的要因の組み合わせによって発生します。[3] [4]高レベルになると、尿酸が結晶化し、結晶が関節、腱、および周囲の組織に沈着して痛風発作を引き起こします。[3]痛風は、ビールや砂糖入り飲料を定期的に飲む人、レバー、貝類、アンチョビなどのプリンを多く含む食品を食べる人、または太りすぎの人によく発生します。 [3] [5]痛風の診断は、関節液中または関節外の沈着物中に結晶が存在することで確定する場合があります。[3]発作中、血中尿酸値は正常な場合があります。[3]
非ステロイド性抗炎症薬(NSAID)、グルココルチコイド、またはコルヒチンによる治療は症状を改善します。[3] [4] [14]急性発作が治まったら、生活習慣を変えることで尿酸値を下げることができ、発作が頻繁に起こる人では、アロプリノールまたはプロベネシドが長期的な予防になります。[7]ビタミンCを摂取し、低脂肪乳製品を多く含む食事を摂ると予防になる場合があります。[15] [16]
痛風は、先進国の成人の約1~2%が人生のある時点で罹患します。[7]痛風はここ数十年でより一般的になっています。[3]これは、メタボリックシンドローム、平均寿命の延長、食生活の変化など、人口におけるリスク要因の増加によるものと考えられています。 [7]最も一般的に罹患するのは高齢男性です。[3]痛風は歴史的に「王の病気」または「金持ちの病気」として知られていました。[7] [17]痛風は少なくとも古代エジプトの時代から認識されていました。[7]
兆候と症状[編集]

痛風はいくつかの形で現れますが、最も一般的なのは急性炎症性関節炎(関節が赤く、痛み、熱を持ち、腫れる)の再発性発作です。[6]親指の付け根にある中足指節関節が最も多く影響を受け、症例の半数を占めています。[12]かかと、膝、手首、指などの他の関節も影響を受ける可能性があります。[6]関節痛は通常夜間に始まり、発症後24時間以内にピークに達します。[6]これは主に体温の低下によるものです。[3]疲労や高熱など、関節痛とともに他の症状がまれに現れることがあります。 [12] [18]
長期にわたる尿酸値の上昇(高尿酸血症)は、痛くない硬くなった尿酸結晶の沈着(痛風結節)などの他の症状を引き起こす可能性があります。痛風結節が広範囲に及ぶと、骨の侵食による慢性関節炎を引き起こす可能性があります。 [19]尿酸値の上昇は腎臓での結晶の沈殿にもつながり、腎結石の形成とそれに続く急性尿酸腎症を引き起こす可能性があります。[20]
原因[編集]
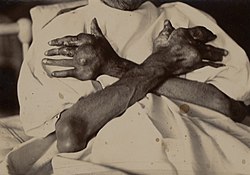
痛風の根本的な原因は、血中の尿酸値が比較的高いことと関係していることが多い尿酸の結晶化です。これは、食事、遺伝的素因、または尿酸の塩である尿酸塩の排泄不足が原因で発生します。 [3]腎臓による尿酸の排泄不足が約90%の症例で高尿酸血症の主な原因であり、過剰産生が原因となる症例は10%未満です。[7]高尿酸血症の人の約10%は、生涯のある時点で痛風を発症します。[21]ただし、リスクは高尿酸血症の程度によって異なります。レベルが415〜530μmol/L(7〜8.9mg/dL)の場合、リスクは年間0.5%ですが、レベルが535μmol/L(9mg/dL)を超える場合のリスクは年間4.5%です。[18]
ライフスタイル[編集]
食事による原因は痛風の約12%を占め、[22] アルコール、砂糖入り飲料、[23]肉、魚介類の摂取と強い関連があります。[6]尿酸値の高いプリンを最も多く含む食品には、干しアンチョビ、エビ、内臓肉、干しキノコ、海藻、ビール酵母などがあります。[24]鶏肉とジャガイモも関連があるようです。[25]その他の誘因には、身体的外傷や手術などがあります。[7]
2000年代初頭の研究では、他の食事要因は関連がないことがわかった。[26] [27]具体的には、適度にプリンを多く含む野菜(豆、エンドウ豆、レンズ豆、ほうれん草など)を含む食事は痛風とは関連がない。[28]食事中の総タンパク質も同様である。[27] [28]アルコール摂取はリスク増加と強く関連しており、ワインはビールや蒸留酒よりもリスクがいくらか低い。[28] [29]グリコマクロペプチド(GMP)とG600乳脂肪抽出物が強化された脱脂粉乳を摂取すると痛みが軽減される可能性があるが、下痢や吐き気を引き起こす可能性がある。[30]
体力、健康的な体重、低脂肪乳製品、そしてそれほどではないがコーヒーやビタミンCの摂取は痛風のリスクを低下させるようです。[31] [32] [33] [34]しかし、ビタミンCサプリメントの摂取は、すでに痛風を発症している人には大きな効果がないようです。[3]ピーナッツ、全粒パン、果物も予防効果があるようです。[25]これは、インスリン抵抗性を軽減する効果があるためだと考えられています。[33]
食事や生活習慣の選択以外にも、痛風発作の再発は天候とも関連しています。気温が高く相対湿度が低いと痛風発作のリスクが高まる可能性があります。[35]
遺伝学[編集]
痛風は部分的に遺伝的であり、尿酸値の変動の約60%に寄与している。[7] SLC2A9 、SLC22A12、およびABCG2遺伝子は、一般的に痛風に関連していることが判明しており、これらの遺伝子の変異はリスクを約2倍にすることができる。[36] [37] SLC2A9およびSLC22A12の機能喪失変異は、尿酸の吸収と拮抗しない尿酸の排泄を減少させることにより、血中尿酸値の低下を引き起こす。[37]まれな遺伝性疾患である家族性若年性高尿酸血症性腎症、髄質嚢胞腎、ホスホリボシルピロリン酸合成酵素過活性、およびレッシュ・ナイハン症候群にみられるヒポキサンチン・グアニンホスホリボシルトランスフェラーゼ欠損症は、痛風を合併する。[7]
病状[編集]
痛風は他の病気と併発することが多い。腹部肥満、高血圧、インスリン抵抗性、異常な脂質レベルが組み合わさったメタボリックシンドロームは、症例の約75%に発生する。[12]痛風によく合併するその他の病状には、鉛中毒、腎不全、溶血性貧血、乾癬、固形臓器移植、多血症などの骨髄増殖性疾患などがある。[7] [38]男性のBMIが35以上の場合、痛風のリスクは3倍に増加する。[26]慢性的な鉛への曝露と鉛に汚染されたアルコールは、鉛が腎機能に有害な影響を与えるため、痛風の危険因子である。[39]
薬物療法[編集]
利尿薬は痛風発作と関連しているが、低用量のヒドロクロロチアジドはリスクを高めないと思われる。[40]リスクを高める他の薬剤には、ナイアシン、アスピリン(アセチルサリチル酸)、ACE阻害薬、アンジオテンシン受容体拮抗薬、β遮断薬、リトナビル、ピラジナミドなどがある。[3] [19]免疫抑制薬の シクロスポリンとタクロリムスも痛風と関連しており、[7]前者はヒドロクロロチアジドと併用するとさらにその傾向が強まる。[41]高尿酸血症はビタミンDサプリメントの過剰摂取によって引き起こされる可能性がある。血清尿酸値は25(OH)Dと正の関連がある。高尿酸血症の発生率は25(OH)Dが10nmol/L増加するごとに9.4%増加した(P < 0.001)。[42]
病態生理学[編集]

痛風はプリン代謝の障害であり、[7]最終代謝産物である尿酸が尿酸ナトリウムの形で結晶化し、関節、腱、および周囲の組織に沈着物(痛風結節)を形成することで発生します。[ 19]顕微鏡的痛風結節はタンパク質のリングで隔てられている場合があり、結晶と細胞の相互作用をブロックして炎症を回避します。[43]関節への軽微な物理的損傷、医療または外科的ストレス、または尿酸値の急激な変化により、隔てられた痛風結節からむき出しの結晶が破れることがあります。[43]結晶が痛風結節を破ると、マクロファージ内でNLRP3インフラマソームタンパク質複合体によって引き起こされる局所的な免疫介在性炎症反応を引き起こします。[3] [19] [43] NLRP3インフラマソームの活性化により、カスパーゼ1という酵素がリクルートされ、プロインターロイキン1βが炎症カスケードの重要なタンパク質の1つである活性インターロイキン1βに変換されます。 [3]尿酸を分解する尿酸酸化酵素(ウリカーゼ)が進化の過程でヒトや高等霊長類で失われたため、この症状は一般的になっています。[7]
尿酸の沈殿の誘因はよくわかっていません。尿酸は正常レベルでも結晶化する可能性がありますが、レベルが上昇するにつれて結晶化する可能性が高くなります。[19] [44]急性関節炎の発作で重要だと考えられている他の誘因には、低温、尿酸値の急激な変化、アシドーシス、関節の水分補給、細胞外マトリックスタンパク質などがあります。[7] [45] [46]低温で沈殿が増えることは、足の関節が最も一般的に影響を受ける理由を部分的に説明しています。[22]尿酸の急激な変化は、外傷、手術、化学療法、利尿剤などの要因により発生する可能性があります。[18]尿酸値を下げる薬の開始または増加は、フェブキソスタットによる特に高いリスクを伴う痛風の急性発作につながる可能性があります。[47] カルシウムチャネル遮断薬とロサルタンは、高血圧の他の薬と比較して痛風のリスクが低いとされています。[48]
診断[編集]
| タイプ | 白血球数(1mm3あたり) | 好中球% | 粘度 | 外観 |
|---|---|---|---|---|
| 普通 | <200 | 0 | 高い | 透明 |
| 変形性関節症 | <5000 | <25 | 高い | クリアイエロー |
| トラウマ | <10,000 | <50 | 変数 | 血まみれ |
| 炎症性 | 2,000~50,000人 | 50~80 | 低い | 曇り黄色 |
| 化膿性関節炎 | >50,000 | >75 | 低い | 曇り黄色 |
| 淋病 | 約10,000 | 60 | 低い | 曇り黄色 |
| 結核 | 約20,000 | 70 | 低い | 曇り黄色 |
| 炎症性:関節炎、痛風、関節リウマチ、リウマチ熱 | ||||
高尿酸血症と足の親指の付け根の典型的な急性関節炎(ポダグラとして知られる)を患っている人では、さらなる検査をしなくても痛風と診断され、治療される可能性があります。診断が疑わしい場合は、滑液の分析を行う必要があります。 [18] [51]単純X線は通常正常であり、初期の痛風の診断を確認するのに役立ちません。[7]骨の侵食などの慢性痛風の兆候が見られる場合があります。[47]
滑液[編集]
痛風の確定診断は、関節液または痛風結節中の尿酸ナトリウム結晶の同定に基づいて行われます。[6]関節穿刺によって診断されていない炎症関節から採取されたすべての関節液サンプルは、これらの結晶がないか検査する必要があります。[7]偏光顕微鏡下では、結晶は針状の形態と強い負の複屈折を示します。この検査は実行が難しく、訓練された観察者が必要です。[52]温度とpHが溶解度に影響を与えるため、液体は吸引後比較的すぐに検査する必要があります。[7]
血液検査[編集]
高尿酸血症は痛風の典型的な特徴ですが、痛風の約半数は高尿酸血症を伴わずに発症し、尿酸値が上昇した人のほとんどは痛風を発症しません。[12] [53]そのため、尿酸値を測定する診断的有用性は限られています。[12]高尿酸血症は、血漿尿酸値が男性で420 μmol/L(7.0 mg/dL)、女性で360 μmol/L(6.0 mg/dL)を超えることと定義されています。[54]一般的に行われるその他の血液検査は、白血球数、電解質、腎機能、赤血球沈降速度(ESR)です。ただし、感染がない場合でも、痛風により白血球とESRの両方が上昇することがあります。[55] [56]白血球数が40.0×10 9 /l(40,000/mm 3)まで上昇したことが記録されています。[18]
鑑別診断[編集]
痛風における最も重要な鑑別診断は化膿性関節炎である。[7] [12]感染の兆候がある人や治療しても改善しない人では、化膿性関節炎を考慮する必要がある。[12]診断を助けるために、滑液のグラム染色と培養が行われることがある。[12]類似する可能性のある他の病状としては、CPPD(偽痛風)、関節リウマチ、乾癬性関節炎、回文性リウマチ、反応性関節炎などがある。[3] [12]痛風結節は、特に関節内にない場合、基底細胞癌[57]や他の腫瘍と間違われることがある。[58]
予防[編集]
痛風発作のリスクは、飲酒を完全に断ち、果糖(高果糖コーンシロップなど)[60]や動物由来のプリンを多く含む食品(内臓肉や魚介類など)の摂取を減らすことで低下させることができます。[ 5 ]乳製品、ビタミンCを多く含む食品、コーヒー、チェリーを食べると痛風発作を予防できる可能性があります。体重を減らすことも痛風発作の予防に役立ちます。[5] [61]痛風は、酸素不足の細胞からプリンが放出されることで睡眠時無呼吸症候群に続発する可能性があります。無呼吸症候群の治療により発作の発生を減らすことができます。[62]
医薬品[編集]
2020年現在、薬物療法を行う場合、アロプリノールは一般的に推奨される予防的治療である。 [63] [64]プロベネシド、フェブキソスタット、ベンズブロマロン、コルヒチンなど、痛風の再発を予防するために、他の多くの薬物療法が時折考慮されることがある。[14] [65] [66]破壊的な関節変化、痛風結節、または尿酸腎症が存在しない限り、痛風発作を2回経験するまで、長期の薬物療法は推奨されない。[ 22 ]この時点で初めて、薬物療法は費用対効果が高くなる。[22]理論上、発作を悪化させる懸念があるため、急性発作が治まってから1~2週間経過するまで、薬物療法は通常開始されない。 [22]最初の3~6か月間は、NSAIDまたはコルヒチンのいずれかと併用されることが多い。[7] [14]
血清尿酸値が300~360μmol/L(5.0~6.0mg/dL)未満になるまで尿酸値を下げる対策を増やすことが推奨されているが、[63] [67]標準用量のアロプリノールを投与するだけよりもこの対策を支持する証拠はほとんどない。[68]発作時にこれらの薬剤を慢性的に使用している場合は、継続することが推奨される。[12]発作が続く間尿酸値を6.0mg/dL未満に下げられない場合は、難治性痛風を示している。[69]
歴史的には、痛風の急性発作中にアロプリノールを開始することは推奨されていないが、この方法は受け入れられているようだ。[70]アロプリノールは尿酸の生成を阻害し、最も一般的に使用されている薬剤である。[22 ]長期療法は安全で忍容性が高く、腎機能障害や尿酸結石のある人にも使用できるが、少数の人に過敏症が起こる。[ 22]ヒト白血球抗原B(HLA-B )の HLA -B*58:01アレルは、アロプリノールによる治療中の重篤な皮膚副作用と強く関連しており、特に韓国人、漢民族、タイ人の子孫であるアジア系集団で最も一般的である。[71]
フェブキソスタットは、アロプリノールに耐えられない人にのみ推奨されます。[72]フェブキソスタットはアロプリノールと比較して死亡率が高いことが懸念されています。[73]フェブキソスタットは、初期治療中に痛風の再発率を高める可能性もあります。[74]しかし、フェブキソスタットはアロプリノールよりも尿酸値を下げる可能性があるという暫定的な証拠があります。[75]
プロベネシドはアロプリノールよりも効果が低いようで、第二選択薬である。[22] [65]プロベネシドは、尿酸の分泌不足(24時間尿中尿酸値800 mg未満)がある場合に使用されることがある。[76]ただし、腎臓結石の既往歴がある場合は推奨されない。[76]プロベネシドはアロプリノールとの併用療法で使用することができ、アロプリノール単独療法よりも効果的である。[77] [78] [79]
ペグロチカーゼは、他の薬剤に耐性のない3%の人々にとっての選択肢です。[80]これは第三選択薬です。[65]ペグロチカーゼは2週間ごとに静脈内注入として投与され、[80]尿酸値を低下させます。[81]ペグロチカーゼは痛風結節を減らすのに役立ちますが、副作用の発生率が高く、多くの人が耐性を獲得します。[65]レシヌラドの使用 400mg+フェブキソスタットは、レシナルよりも痛風結節の解消に効果的である。フェブキソスタットと併用して200mLを服用すると、同様の副作用がみられる。レシナルとアロプリノールの併用は痛風結節の解消には効果がない。[82]潜在的な副作用としては、腎結石、貧血、関節痛などがある。[83] 2016年に欧州市場から撤退した。[84] [85]
レシヌラドは腎臓での尿酸の吸収を防ぐことで血中尿酸値を下げます。[86]米国では尿酸値の目標値に達しない人に対してアロプリノールとの併用が承認されました。[87]副作用には腎臓障害や腎臓結石などがあります。[86] [88]
治療[編集]
治療の第一の目的は、急性発作の症状を鎮めることである。[89]血清尿酸値を下げる薬を服用すれば、再発を予防できる。[89]痛みを軽減するために、1日に数回、20~30分間氷を当てることが暫定的な証拠から支持されている。[90]急性治療の選択肢としては、非ステロイド性抗炎症薬(NSAID)、コルヒチン、グルココルチコイドなどがある。[22]グルココルチコイドとNSAIDはどちらも効果は同等だが、グルココルチコイドの方が安全かもしれない。[91]予防の選択肢としては、アロプリノール、フェブキソスタット、プロベネシドなどがある。尿酸値を下げることで、この病気を治すことができる。[7]関連する健康問題の治療も重要である。[7]生活習慣への介入については十分に研究されていない。[90]痛風患者に栄養補助食品が効果があるかどうかは不明である。[92]
NSAIDs [編集]
NSAIDsは、痛風の通常の第一選択薬です。特定の薬剤が他の薬剤よりも著しく効果的または効果的でないということはありません。[22]改善は4時間以内に見られる場合があり、1~2週間の治療が推奨されます。[7] [22]消化管出血、腎不全、心不全などの特定の健康上の問題を抱えている人には推奨されません。[93]インドメタシンは歴史的に最も一般的に使用されているNSAIDですが、優れた有効性がない場合には副作用プロファイルが優れているため、イブプロフェンなどの代替薬が好まれる場合があります。 [40] NSAIDsによる胃の副作用のリスクがある人には、追加のプロトンポンプ阻害剤が投与される場合があります。[94] COX-2阻害剤は、急性痛風発作に対して、副作用が少なく、非選択的NSAIDsと同様に効果がある可能性があるという証拠がいくつかあります。 [95] [96] [97] [98]
コルヒチン[編集]
コルヒチンは、 NSAIDsに耐えられない人のための代替薬です。[22]高用量では、副作用(主に胃腸障害)により使用が制限されます。[99]低用量でも効果があり、忍容性は良好です。[40] [100] [97] [98]コルヒチンは、アトルバスタチンやエリスロマイシンなど、他の一般的に処方される薬剤と相互作用する可能性があります。[99]
グルココルチコイド[編集]
グルココルチコイドはNSAIDsと同等の効果があることがわかっており[96] [101]、NSAIDsの禁忌がある場合に使用できる。[22] [102]また、関節内に注射すると症状が改善する。[22]ただし、グルココルチコイドは関節感染症を悪化させるため、関節感染症を除外する必要がある。[22]短期的な副作用は報告されていない。[103]
その他[編集]
カナキヌマブなどのインターロイキン-1阻害剤は、鎮痛や関節の腫れの軽減に中程度の有効性を示したが、腰痛、頭痛、血圧上昇などの有害事象のリスクが高まった。 [104]しかし、NSAIDの通常の用量よりも効果が低い可能性がある。[104]このクラスの薬剤はコストが高いため、痛風の治療に使用されない可能性もある。[104]
予後[編集]
治療しなければ、痛風の急性発作は通常5~7日で治まりますが、60%の人が1年以内に2度目の発作を起こします。[18]痛風患者は高血圧、糖尿病、メタボリックシンドローム、腎臓疾患や心血管疾患のリスクが高く、死亡リスクも高くなります。[7] [105]尿酸値を下げる薬が心血管疾患のリスクに影響するかどうかは不明です。[106]これはインスリン抵抗性や肥満との関連が一因かもしれませんが、リスク増加の一部は独立しているようです。[105]
治療しないと、急性痛風発作は慢性痛風に発展し、関節面の破壊、関節変形、無痛性の痛風結節が生じることがあります。[7]これらの痛風結節は、5年間治療を受けていない人の30%に発生し、耳介、肘頭突起の上、またはアキレス腱によく発生します。[7]積極的な治療を行えば、痛風結節は溶解する可能性があります。また、腎臓結石が痛風を合併することが多く、10~40%の人が罹患しており、尿のpHが低く尿酸の沈殿を促進するために発生します。[7]他の形態の慢性腎機能障害が発生することもあります。[7]
疫学[編集]
痛風は、西洋世界では生涯のある時点で約1~2%の人に影響を与えており、より一般的になりつつあります。 [7] [22] 2013年には約580万人が罹患しました。[107]痛風の発生率は、1990年から2010年の間に約2倍になりました。[19]この増加は、平均寿命の延長、食生活の変化、メタボリックシンドロームや高血圧など痛風に関連する疾患の増加によるものと考えられています。[26]痛風の発生率に影響を与える要因には、年齢、人種、季節などがあります。30歳以上の男性と50歳以上の女性では、発生率は2%です。[93]
米国では、アフリカ系男性はヨーロッパ系男性に比べて痛風の発症率が2倍高い。[ 108]ポリネシア人では発症率が高いが、オーストラリア先住民では、後者のグループでは平均尿酸血清濃度が高いにもかかわらず、この病気はまれである。 [109]中国、ポリネシア、サハラ以南のアフリカの都市部では痛風が一般的になっている。[7]いくつかの研究では、痛風の発作は春に多く起こることがわかっている。これは、食事、アルコール摂取、身体活動、気温の季節的な変化に起因するとされている。[110]
歴史[編集]

英語の「痛風」という語は、1200年頃のボッキングのランドルフスの著作に初めて登場します。[112] これはラテン語の「一滴」(液体)を意味するguttaに由来しています。 [111]オックスフォード英語辞典によると、これはユーモア主義と「関節の周りの血液から病的な物質が『滴り落ちる』という概念」に由来しています。[113]
痛風は古代から知られています。歴史的に、賢者はこれを「病気の王であり、王の病気」[7] [114]または「金持ちの病気」と呼んでいました。[17]エーベルス・パピルスとエドウィン・スミス・パピルス(紀元前 1550年頃)は、それぞれ第1中手指節関節の関節炎を独特のタイプの関節炎として言及しています。これらの古代の写本は、1,000年前に書かれたとされ、イムホテプに帰せられる痛風に関するエジプトのテキスト(現在は失われています)を引用しています。[115] 紀元前400年頃のギリシャの医師ヒポクラテスは、彼の格言の中で 、宦官と閉経前の女性には痛風がないことを指摘しています。[111] [116] アウルス・コルネリウス・セルス(紀元30年)は、アルコールとの関連性、女性に後から発症すること、それに伴う腎臓の問題を次のように記述している。
イギリスの医師ベンジャミン・ウェルズは1669年に痛風に関する最初の医学書『痛風あるいは関節炎の論文』を著した。 [118] 1683年にはイギリスの医師トーマス・シデナムが痛風が早朝に発症し、高齢男性に多いことを記述した。
18 世紀にトーマス・マリアットは痛風のさまざまな症状を区別しました。
オランダの科学者アントニー・ファン・レーウェンフックは1679年に初めて尿酸結晶の顕微鏡的外観を記述した。 [111] 1848年にイギリスの医師アルフレッド・ベアリング・ギャロッドは、血液中の過剰な尿酸が痛風の原因であると特定した。[121]

![偏光された尿酸結晶は負の複屈折を示し、赤色補償器の軸に平行に並ぶと黄色になり、垂直に並ぶと青色になる。[59]](https://upload.wikimedia.org/wikipedia/commons/thumb/b/b2/Birefringence_microscopy_of_gout%2C_annotated.jpg/200px-Birefringence_microscopy_of_gout%2C_annotated.jpg)









コメント
コメントを投稿